1/13ページ
ダウンロード(4.2Mb)
化学反応のメカニズムと反応経路を理解するための情報収集に、In Situ FTIRがいかに効果的であるかご説明します。
・ホワイトペーパー 「有機化学の進歩 - 金属触媒による変換反応」では、さまざまな化学反応のメカニズムと反応経路を理解するための情報収集に、In Situ FTIRがいかに効果的であるかご説明します。また有機化学における最近動向についても述べています。
・核磁気共鳴 (NMR) 分光法などによる他の構造データを、In Situ FTIR分光法を使用して収集した情報でどのように補完できるか。
・従来の手法よりも少ない実験で化学反応の反応速度情報を精査する高度な手法が、In Situ FTIRと反応速度解析ソフトウェアの組み合わせからどのようにして得られるか。
このカタログについて
| ドキュメント名 | 有機化学の進歩 |
|---|---|
| ドキュメント種別 | ホワイトペーパー |
| ファイルサイズ | 4.2Mb |
| 取り扱い企業 | メトラー・トレド株式会社 (この企業の取り扱いカタログ一覧) |
この企業の関連カタログ

このカタログの内容
Page1
有機化学の進歩
In Situ 分光法を用いた最新研究のご紹介
金属触媒による変換反応
Adrian Burke, Dominique Hebrault, METTLER TOLEDO
金属触媒による変換反応が学 In Situ赤外分光法の有機合成 です。大量のデータを自動採取
術研究における重要なトピック 化学への活用に拍車がかかっ することで正確な反応速度解析
となって久しく、科学的な関心 ているのは、広範な反応に適用 が可能となるとともに、専用ソフ
事としてだけでなく、産業面に でき、反応機構・反応速度・反応 トウェアiC KineticsTMが従来手
おいても貴重な反応として実用 経路の解明に役立つ貴重な情 法より少ない実験数で反応速度
化されてきています。そして今日 報が得られるからです。 モデルを生成します。
、研究者にとって大きな課題と
なっていることは、反応開始点 ReactIRTMは合成反応をリアルタ この解説書で取り扱う4つの
と終点の正確な把握など化学 イムに In Situで分析する装置 アカデミアによる研究例では、
反応の詳細な理解や、特性評価 であり、有機合成反応の詳細な ReactIRTMを用いることで研究上
および最適化を目的とした正確 解明のために用いられます。実 重要なデータや新たな知見を
なデータの採取であると言われ 績豊富な中赤外分光法で反応 得ています。本解説書はご紹介
ています。少人数で短期間に大 中の化学物質を捉えます。堅牢 する各文献の科学的発見につ
量の研究を遂行せねばならな なATRプローブを反応器に直接 いて詳しく説明するものではあ
い企業の経済的なニーズもあ 挿入しリアルタイムで採取され りませんので、それらはオリジ
いまって、研究を成功に導くこと るスペクトルは、まさに反応中の ナルの文献をご参照ください。
ができるデータを採取すべく、革 「分子の動画」と言えます。主要 ここではReactIRTMの利用法と、
新的な研究法が模索されてい な反応物、過渡種すべての濃度 その結果いかに研究課題が解
ます。 変化を追跡することで、反応機 決されたかを詳細にご説明い
構や反応経路を解明できるの たします。
Page2
1. Bi‐Rhヘテロ二核金属Paddle-
wheel型カルボキシラートを触媒
とした金属カルベノイド変換反応
Jørn Hansen†, Bo Li‡, Evgeny Dikarev‡, Jochen Autschbach§
and Huw M. L. Davies*†
† Department of Chemistry, Emory University, 440 Atwood Hall, 1515 Dickey
Drive, Atlanta, Georgia 30322 ‡ Department of Chemistry, University at Albany,
State University of New York, Albany, New York 12222 § Department of Chemis-
try, University at Buffalo, State University of New York, Buffalo, New York 14260-
3000 J. Org. Chem., 2009, 74 (17), pp 6564–6571
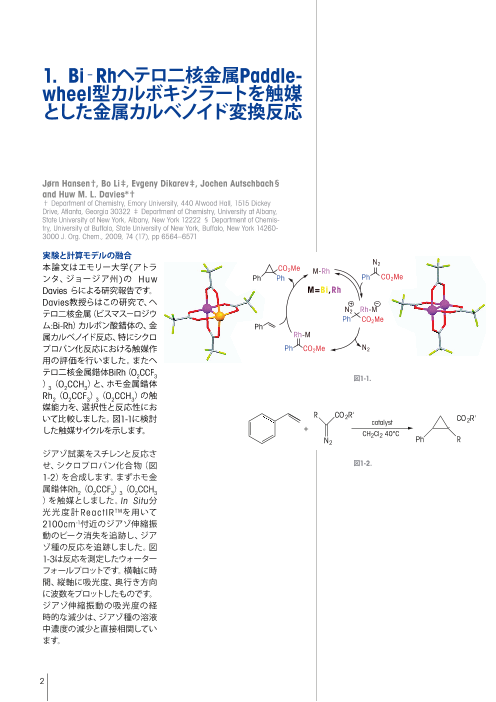
実験と計算モデルの融合
N
本論文はエモリー大学(アトラ 2CO2Me M-Rh
ンタ、ジョージア州)の Huw Ph Ph Ph CO2Me
Davies らによる研究報告です。 M=Bi,Rh
Davies教授らはこの研究で、ヘ
テロ二核金属(ビスマス-ロジウ N2 Rh-M
Ph CO Me
ム:Bi-Rh)カルボン酸錯体の、金
2
Ph
属カルベノイド反応、特にシクロ Rh-M
プロパン化反応における触媒作 Ph CO2Me N2
用の評価を行いました。またヘ
テロ二核金属錯体BiRh(O2CCF3 図1-1.
)3(O2CCH3)と、ホモ金属錯体
Rh2(O2CCF3)3(O2CCH3)の触
媒能力を、選択性と反応性にお
いて比較しました。図1-1に検討 R CO2R' catalyst CO2R'
した触媒サイクルを示します。 + CH2Cl2 40°C
N2 Ph R
ジアゾ試薬をスチレンと反応さ
せ、シクロプロパン化合物(図 図1-2.
1-2)を合成します。まずホモ金
属錯体Rh2(O2CCF3)3(O2CCH3
)を触媒としました。In Situ分
光光度計Reac t IR TMを用いて
2100cm-1付近のジアゾ伸縮振
動のピーク消失を追跡し、ジア
ゾ種の反応を追跡しました。図
1-3は反応を測定したウォーター
フォールプロットです。横軸に時
間、縦軸に吸光度、奥行き方向
に波数をプロットしたものです。
ジアゾ伸縮振動の吸光度の経
時的な減少は、ジアゾ種の溶液
中濃度の減少と直接相関してい
ます。
2
Page3
0.144
-0.033
O O
21 059 F C 0:00:3 R5h6 CF3
Waven TimOe Oumber (cm-1) 200
0
6 0:00:11 O OF3C CH Bi 3O O
0.144 0.215
-0.033 -0.018
21 0
01:0
5 0: 29 00:56 185
1:48
Wave Time Wnu am ve Ti
me
b ne ur m (cm-1 200 06 0
b
:0 e0 r: () 11 cm-1)
198 00 0:00:02
0.215
図1-3のウォーターフォールプロットは、反応が非常に高速であるこ 図1-3(左) 図1-4(右)
とを示しており、実際、図で示した時間幅すなわち56秒で終結して
います。触媒量は0.2mol%でありターンオーバー頻度は約30s-1に
-0.0
相当します。 18
21 08 1:5 01:48
一方、図1-4Wはaveヘn テロ金属錯体BiRh(O2CCFT3i)m(3eOum 2
CCH3)を触媒とし
て用いた結果ですb。er同 (cm様-1)の1980条件
00下:00:0で2 反応しましたが、ホモ金属錯体
に比べ反応が大幅に遅くなりました。実際に反応が完了するまで45
分程度かかり、ターンオーバー頻度は約0.019s-1でした。
このデータで2つの触媒の相対的な反応性を直接、比較できます
。ホモ金属錯体Rh(2 O2CCF3)(3 O2CCH3)はヘテロ金属錯体BiRh(
O2CCF3)(3 O2CCH3)よりも約1600倍以上反応性が高いことがわかり
ます。これは計算モデルの結果と合致しました。
この実験例から、In Situ反応分析装置ReactIRTMにより、きわめて容
易に反応時間を数値化できることがわかります。反応液に ReactIRTM
プローブを直接浸し、ジアゾ化合物の消失速度をモニタリングした
にすぎません。図1-3と図1-4のように、その濃度減少をグラフで視
覚化しただけで、反応時間はそれぞれ16秒と45分であることが容
易に読み取れます。またReactIRTMの高速スキャンモードでは、1秒
毎のスペクトル採取が可能であり、非常に速い反応においても進行
状況を追跡することができます。
3
A.U. A.U.
A.U. A.U.
Page4
2. 2 -リチオ-3,3 -ジメチル-2 -オ
キサゾリニルオキシラン:カルバ
ニオンか?アザエノラートか?
Vito Capriati*, Saverio Florio*, Renzo Luisi, Filippo Maria Perna
and Agnese Spina
Dipartimento Farmaco-Chimico, Università di Bari, Consorzio Interuniversitario
Nazionale Metodologie e Processi Innovativi di Sintesi C.I.N.M.P.I.S., Via E. Orabona
4, I-70125 Bari, Italy; J. Org. Chem., 2008, 73 (24), pp 9552–9564.
溶液中の構造・立体配置安定性・立体ダイナミクス
In Situ赤外分光光度計ReactIRが化学反応をモニ O Me
タリングするだけでなく、反応中間体の構造推定 Li
に役立つデータを提供した、優れた実験例をご紹 N Me
介します。イタリアのバーリ大学の Vito Capriati と O
Saverio Florio らは、In Situ赤外分光光度計とNMR azaenolate
を使って図2-1に示すリチウム塩の安定性に関する
新しい知見を得ました。これまでの研究では、結
図2-1.
果に矛盾がありました。まずリチウム塩は超低温
において高速でラセミ化するというコンピュータ
モデリングからの結果がありました。一方、それに
反し重水素化実験においては、同じ分子が-78℃
でも安定していることが観察されたのです。
H O Me Li O Me
s-BuLi/TMEDA
図2-2は、化合物1を-100℃のTHF中で強塩基と反 N Me THF, -98°C N Me
応させリチウム塩Li-1を合成するスキームです。 O O
本件において特に重要であったのは、「リチウム塩 1 Li-1
は有機リチウムなのか、あるいはアザエノラート
なのか?」という疑問に答えることでした(図2-3)。 図2-2.
? O MeN Li
O O Me N Me
O
Li Me
Li-1
organolithium azaenolate
図2-3.
3b. hydrated form of carbamazepine
4
Page5
In Si tu赤外分光法から興味深
い手がかりが得られました。脱
プロトン化が起きると、化合物1 H O Me Li O Mes-BuLi/TMEDA
のオキサゾリニル種に相当する N Me THF, -98°C N Me
1660cm-1と1678cm-1の2吸収が O 1 O Li-1
消え、その時1600cm-1の吸収が
出現しているのです(図2-4)。 Band at 1600cm-1
文献データによれば、図2-3のア Absorbance
ザエノラートのような構造のア Bands at 1660 and 1678cm
-1
ルキリデンエポキシドは、1750 0.04
~1800cm-1の領域に吸収を持 0.03
つことが多いとされています。 0.02
本件では反応後、低波数側へ
0.01
60cm-1程度しかシフトしないこ
とから、有機リチウム誘導体Li-1 0.00
が形成されていることを示唆し -0.02
ていると言えます。 1700 1680 1660 1640 1620 1600 1580
Wavenumber (cm-1)
前章の Huw Davies らの研究と
同様、これは非常に速い反応で 図2-4.
す。化合物1は1分以内に全て反
応していることが、化合物1とリ
チオ化した等価物の吸収の時間
変化から見て取れます(図 0.042.5)。
Compound 1
Compound 1
In Situ中赤外分光法により、官能 0.03 Compound Li-1
基の吸光特性に基づいた重要な
情報を採取することで、疑わしい
アザエノラートではなく、Li-1の 0.02
形成を示唆する情報が得られま
した。研究者らは後日、13C 7Li 0.01
NMRによって反応中間体を研究
し、この結果が正しいことを確
認しました。 0
0 20 40 60 80 100
Time (min)
図2-5.
5
Absorbance
Page6
3.パラジウム触媒によるホスフィ
ン-オレフィン配位子を利用した
効率の良いC(SP)-C(SP)クロ
スカップリング反応P
Wei Shi†, Yingdong Luo†, Xiancai Luo†, Lei Chao†, Heng
Zhang†,
Jian Wang‡ and Aiwen Lei*†
College of Chemistry and Molecular Sciences, Wuhan University, Wuhan, Hubei
430072, P. R. China, and Mettler-Toledo AutoChem, 7075 Samuel Morse Drive,
Columbia, Maryland 21046; J. Am. Chem. Soc., 2008, 130 (44), pp 14713–
14720; † Wuhan University,
‡ Mettler-Toledo AutoChem, Inc.
アプリケーションと反応メカニズムの観点 Pd (dba)2/L1
武漢大学(中国・北京)のAiwen Leiとメトラー・トレ NEt 3, Cul
ド・オートケムは、Pd触媒を用いたクロスカップリ R1 Br + R2 R1 R2DMF, r.t., 2-9h
ング反応による、ハロアルキン1と末端アルキン2 1 2 3
からの、ジイン3の合成に関する共同研究を行い
ました(図3-1)。本稿では、In Situ赤外分光法によ
り様々な条件下で反応速度を測定し反応機構の PPh2
解析を行いました。根岸カップリングに関して同 L1=
様の反応機構的アプローチを行った同じ著者の
報告もあります5。
O
この化学反応により、1,3 - ジインを非常に効 図3-1.
率的に合成することができます。図3-2に示した
ように、ブロモアルキン1とジイン3はそれぞれ
973cm-1と955cm-1に特異な吸収を持っています
。図3-3に示したこれら吸収の時間変化プロットに
より、出発物質と生成物の反応中の濃度変化が一
目でわかります。
1c= Br OH 3a=
OH
3a
3a -1
0.15 3a
955cm
955cm-1
955cm-1 1c 0.05
1c 973c1cm-1
973cm-1 0.04973cm-1
0.10 0.03
0.02
0.01
0.05 0.00
0:48:00
0:28:00
0.00 0:08:00
1000 980 960 940 985 975 965 955 945
Wavenumber (cm-1) Wavenumber (cm-1)
図3-2. (左) 図3-3. (右)
6
Absorbance
Time/min
Absorbance
Page7
1.0E4
0.4
9.6E4
0.3
9.2E4
0.2
Reaction A 8.8E5
0.1 Reaction B
8.4E5
0
8.0E5
0 50 100 150 0.03 0.08 0.13 0.18
Time (min) R-Br
a. b.
図3-4.
次にBlackmondの反応速度解析法6,7を用いて、2つ
の反応条件を入念に設定し、実験を行いました。反
応Aと反応Bは、触媒量は一定のまま反応物の濃度
が異なり、またそれぞれフェニルアセチレンが過剰量
(0.02M)となっています。
Reactant Concentrations
Reactants ReactionA ReactionB
OH
Br 0.41M 0.29M
OH OH
Ph 0.43M 0.31M Cul (0.003M)Ph + Br PhPd(dba)2(0.006M)
2g 1c 3a
Pd(dba)2 0.006M 0.006M [2g] = 0.43M [1c] = 0.29M
[1c] = 0.47M
[1c] = 0.41M
CuI 0.003M 0.003M
図3-4aは3aの濃度の時間変化グラフです。図3-4b
は同じデータから、ブロモアルキンの濃度と反応速 100
度の関係をプロットとしたものです。2つのプロット
が完璧に重なっており、触媒の失活や阻害が無いこ 80
とを示しています。
60
1c with 2g
続いて3つ目の実験は、ブロモアルキン1の濃度のみ 40 1a with 2a
変化させ、他は同じ条件にて行いました(異なる過
剰量での実験)。図3-5aから、反応の初期速度に違 20
いは見られません。またゼロ次反応のように見えま 0
す。図3-5bにおいて、調整された濃度に対して正規
化した反応速度をプロットすると、上記の観察結果 0 50 100 150 200
が裏付けられました。もっとも直線性を示す反応係 Time
数は、末端アルキンで0.07およびブロモアルキンで
0.03でした。 図3-5a.
7
[3a] (mol/L)
Conversion (%)
Rate
Page8
これらの結果を考察すると、触媒サイクル内のブ
ロモアルキンと末端アルキンのいずれも律速段階
に関与しないことが示唆されています。
結果として、この触媒サイクルに関する2つの疑問
が浮上しました。すなわち律速段階はどこか、また
、中間体4と5が縮合して6になるのか、あるいは還
元的脱離で最終生成物3ができるのかということ
です(図3-6)。
この論文は、In Situ赤外分光法でデータを採取す
ると共に、反応条件を巧みに計画し実験を行うこ
とによって、上記クロスカップリング反応の反応機
構に関する重要な知見を提示しました。さらに数
回の実験を行い、還元的脱離段階が律速であるこ
とと、図3-1に示したリガンドL1の存在による反応性
図3-5b.
の向上を明らかにしています。
Pd(L1)
R1 R2
3 2 R1 Br
1
Two pos-
sible rate-
limiting
steps
R1 Pd(L1) R
1 Pd (L1)
6 4 Br
1
2
R2 Cu R5
CuBr HNEt 3 'Br
H R3 NEt 3
2
図3-6.
ウェビナーご紹介
Reaction Progress Kinetic Analysis:
複雑な触媒反応機構を解明する強力な手法
Reaction Progress Kinetic Analysis(RPKA)を用いて有
機反応の速度論研究を単純化する手法について、Donna
Blackmond 教授がご説明します。RPKA法の利点は、新規
反応においてもごく初期の実験から、重要な速度情報を迅
速に算出・抽出でき、その後の反応の最適化と、他法による
根本的な反応機構研究の方向性を得られることにあります。
無料オンラインセミナーはこちらから
www.mt.com/iCKinetics
8
Page9
4. C = C結合を有するシクロペン
タジエニルルテニウムアルコキシ
カルボニル錯体の予期せぬ生成
Jenny B. Åberg, Madeleine C. Warner and Jan-E. Bäckvall*
Department of Organic Chemistry, Arrhenius Laboratory, Stockholm University,
SE-106 91 Stockholm, Sweden; J. Am. Chem. Soc., 2009, 131 (38), pp 13622–
13624
ルテニウム錯体触媒による動的 OH OAc Ph Ph
速度論分割 cat. 1, cat. t-BuOK
ルテニウム触媒はリパーゼと組 PhR R
み合わせ、ラセミ第二級アルコー CALB, Ph
ル2からエナンチオ選択的に酢
Ru
OAc Ph CO
酸塩3へ変換させることから、動 racemic toluene R-acetate CO CO
的速度論分割(dynamic kinetic 1
resolution:DKR)と呼ばれてい 2 R=large 3 R=large high yield
ますが、オレフィンアルコール4 group group high ee(alkyl, aryl) (alkyl, aryl)
にはうまく働きません。アルコー 4 R=H2C=CHCH2CH2
ル4の二重結合がルテニウムと 5 R=H2C=CHCH2CH2
配位するのが原因で、ラセミ化 <50%; no DKR
が非常に遅いのではないかとい
う仮説も考えられていました。こ
の論文はNMR分光法とIn Situ赤 1982cm-1
-1
外分光法を使用し、ルテニウム 2021cm-1 1644cm-1
(Ru-O t - B u 6 ) 1964cm
―オレフィン錯体の存在を明ら (Ru-Ot -Bu6)
かにします。 T= 29min
T= 0 min
0.03
アリルアルコールとルテニウム錯
体が反応するとき、2021cm-1と
1964cm-1の2本の赤外吸収が時 0.02
間とともに減少します。これらは
ルテニウム錯体1に由来するピー
クです。新しい吸収はCO領域の 0.01
1982cm-1に現れます。またアシ
ル領域に1644cm-1のピークも現
れます(図4-1)。 0
2040 1960 1880 1800 1720 1640
Wavenumber (cm-1)
図4-1.
9
Reaction Spectra (A.U.)
CO Region
Acyl Region
Page10
Backvallらはこれらピークの時
間変化を検討し(図4-2)、消失
と形成の速度が同じであること Alcohol 4 Addition
から、ジアステレオマー10a-bが
形成されているという仮説を裏
1644cm-1
付けました(図4-3)。 0.03 1982cm-1
1964cm-1
2021 cm-1
この研究は、官能基に特異的な
中赤外吸収による構造情報と、 0.02
In Situ反応速度モニタリングか
ら得られた速度情報を融合す
ることにより、優れた結果が得 0.01
られる実証となりました。最終
的にはIn Situ赤外分光法に加え
て1H 13C NMR分光法を用い、ジ 0
アステレオマールテニウム錯体
10a-bの形成を確認することが 00:20:00 00:30:00 00:40:00 00:50:00
できました。また、アルコール4 Relative Time (mins)
のラセミ化が遅く、それが動的
速度論分割がうまく進行しない
理由であることを証明するデー 図4-2.
タとなりました。
Ph Ph
10a-b
Ph 6
Ph 5
Ph Ru 4
OC C
3
O O 2
図4-3.
1
10
Reaction Spectra (A.U.)
Page11
®
PVMまとめ
™
ctIR
Rea
序文で述べたとおり、この解説書は各論文における科学的知見
を詳細に解説することが目的ではありません。In Situ分光光度計
ReactIRTMを単独もしくは他の技術と組み合わせて使用することで、 ®
反応速度・反応経路・反応機構の解明のための重要な手がかりが FBRM
得られることを、好例からご理解いただければ幸いです。
iC
Software
ALR
事例からのまとめ
- In Situ分光光度計ReactIRTMにより、様々な化学反応の
反応機構・反応経路を解明するにあたって有用で相補 メトラートレドについて
的な情報を得ることができる。 メトラートレドは、世界的ネットワー
- In Situ分光光度計ReactIRTMで採取した情報は、 の
クを有し、各国の技術アプリケーシ
NMR ョンコンサルタントが、お客様の有
ような他の構造解析結果を高度に補完することができ 機合成、化学品開発、スケールアッ
る。 プをサポートする広範な知見をご提
- In Situ分光光度計ReactIRTMとiC KineticsTMソフトウェア 供します。
の併用は、従来法に比べ少ない実験数で化学反応の速 Email: autochem@mt.com
度論研究が可能な、革新的手法である。 Phone: 410-910-8500
Website
メトラートレドのホームページに
オートケムのページがございま
す。(www.mt.com/autochem)
製品やアプリケーションに関する詳
細な情報や、多くの最新オンデマン
ドウェビナーのリストがご覧いただ
けます。
ブログ
Chemical Research, Development
and Scale-upブログは、最新の文献
情報や、弊社技術者および官学民の
研究者による専門的なコメントを掲
載しています。
カスタマーコミュニティ
カスタマーコミュニティサイトには、
弊社装置をお持ちのお客様が自由
にアクセスしていただき、文献リスト
やアプリケーションレポート、実例
集、トレーニング資料をご利用いた
だけます。こちらからオンデマンドの
ウェビナーにもアクセスできます。
ソーシャルメディア
FacebookとTwitterでも化学合成、
化学工学、スケールアップに関する
最新情報をアップデートしています。
11
Page12
付録:文献リスト
1. Jørn Hansen, Bo Li, Evgeny Dikarev, Jochen Autschbach and Huw M. L. Davies*,
Combined Experimental and Computational Studies of Heterobimetallic Bi-Rh
Paddlewheel Carboxylates as Catalysts for Metal Carbenoid Transformations, J.
Org. Chem., 2009, 74 (17), pp 6564–6571.
2. Vito Capriati*, Saverio Florio*, Renzo Luisi, Filippo Maria Perna and Agnese Spina,
2-Lithio-3,3-dimethyl-2-oxazolinyloxirane: Carbanion or Azaenolate? Structure,
Configurational Stability, and Stereodynamics in Solution, J. Org. Chem., 2008, 73
(24), pp 9552–9564.
3. Wei Shi, Yingdong Luo, Xiancai Luo, Lei Chao, Heng Zhang, Jian Wang and Aiwen
Lei*, Investigation of an Efficient Palladium-Catalyzed C(sp)-C(sp) Cross-Coupling
Reaction Using Phosphine-Olefin Ligand: Application and Mechanistic Aspects, J.
Am. Chem. Soc., 2008, 130 (44), pp 14713–14720.
4. Jenny B. Åberg, Madeleine C. Warner and Jan-E. Bäckvall*, Unexpected Formation
of a Cyclopentadienylruthenium Alkoxycarbonyl Complex with a Coordinated C═C
Bond, J. Am. Chem. Soc., 2009, 131 (38), pp 13622–13624.
5. Aiwen Lei et al: Org. Lett. 2008, 10, (13), 2661-2664.
6. Donna G. Blackmond, Angew. Chem. Int. Ed. 2005, 44, 4302 – 4320.
7. Reaction Progress Kinetic Analysis: A Powerful Methodology for Streamlining the
Study of Complex Organic Reactions, Donna G. Blackmond, Webinar, www.mt.com/
ac-webinars
12
Page13
ReactIRおよび関連装置のご紹介
In Situ FTIR反応解析装置 ReactIRTM
ReactIR™ は、試料採取を必要とせず、重要な反応
化学種をモニタリングするリアルタイム組成分析装
置です。In Situでリアルタイムに反応をモニタリング
しますので、反応を高度に解析するための最大限
のデータを、最小の労力で手にすることができます。
www.mt.com/autochem
www.mt.com/ReactIR
Adrian Burke, BSc (Hons)
Adrian_Burke@mt.com
iC KineticsTM
iC KineticsTMはグラフィックで化学反応の迅速な理
解と最適化を支援するソフトウェアです。速度モデ
ルを生成し、濃度と温度が反応性に及ぼす影響を
シミュレートできます。従来法より少ない実験数で
データを生成しますので、迅速な反応条件の最適
化に寄与します。
www.mt.com/iCKinetics
EasyMaxTM
EasyMaxTM 必要な反応物の量に合わせ、反応器と
反応条件を組み換えられる自動合成装置です。複
数の反応条件・出発物質を迅速に評価できます。
容量の異なる反応器で、完全に独立した実験を同
時に行うことができ、迅速でより信頼性の高い合
成が可能となります。
www.mt.com/EasyMax
お客様の研究に最適な装置についてメトラートレドまでご相談ください
メトラー・トレド株式会社 オートケム事業部
TEL:03-5815-5515 FAX:03-5815-5525
©1/2014 Mettler-Toledo K.K.,